新型非洲猪瘟候选疫苗取得新进展:强毒下实验猪群100%存活!

---- 广告,也是一种资讯----
近日,我国科研团队在非洲猪瘟(ASF)疫苗研发中取得重要进展。一种同时缺失CD2v和A137R基因的减毒活疫苗候选株,在实验猪群中表现出良好的安全性和免疫保护效果,能够完全抵抗同源强毒株的攻击。该研究由中国兽医药品监察所与中国科学院微生物研究所等单位合作完成,已于近期在学术期刊《Journal of Virology》上发表。

非洲猪瘟仍是全球养猪业的“心头大患”
非洲猪瘟自2018年传入中国以来,对我国养猪业造成巨大冲击。该病由非洲猪瘟病毒(ASFV)引起,发病急、死亡率高,目前尚无商业化疫苗可用。传统防控手段依赖扑杀和生物安全措施,不仅成本高昂,也给养殖户带来沉重负担。
因此,开发安全有效的疫苗,成为行业迫切需求。减毒活疫苗因其能同时激发体液免疫和细胞免疫,被广泛认为是防控ASF最有希望的疫苗类型。
突破:双基因缺失病毒株诞生,安全有效
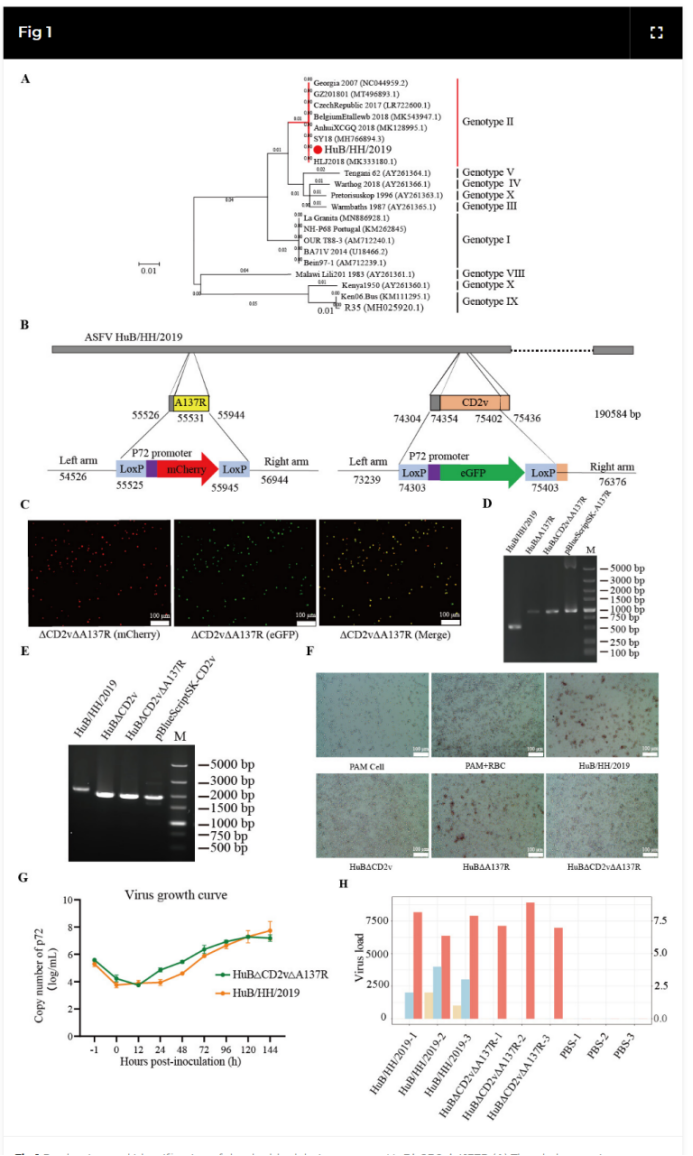
研究人员从一株分离自湖北的强毒株ASFV HuB/HH/2019(属于基因II型)出发,利用基因编辑技术同时敲除了CD2v和A137R两个基因,成功构建出双基因缺失病毒株HuBΔCD2vΔA137R。
CD2v蛋白与病毒吸附红细胞、形成“玫瑰花环”现象有关,并能抑制宿主干扰素应答;A137R蛋白则是病毒颗粒的结构蛋白,同样具有抑制Ⅰ型干扰素的作用,且其抗体还可能增强病毒感染(即抗体依赖性增强作用,ADE)。缺失这两个基因后,病毒毒力显著降低,同时保留了良好的免疫原性。
无毒、无热、无死亡,保护率100%
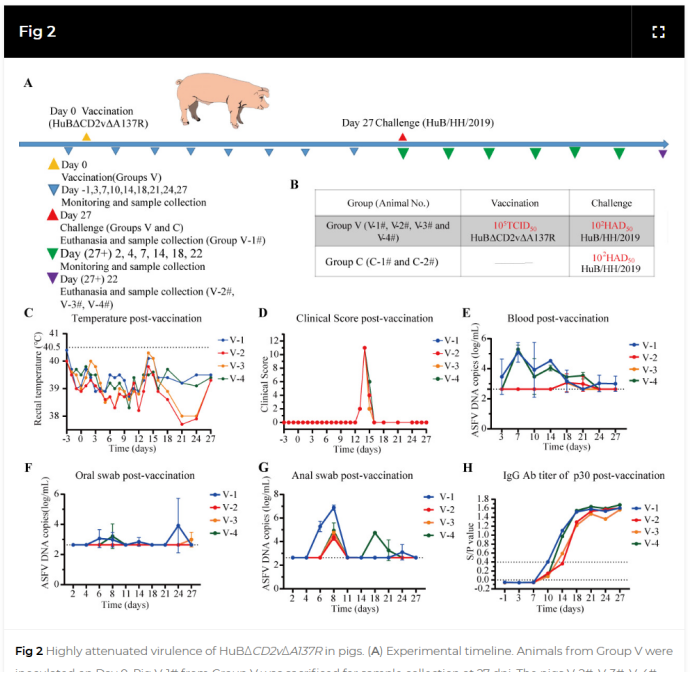
在动物实验中,4头猪接种10^5 TCID₅₀剂量的双缺失病毒后,在27天观察期内全部存活,仅2头出现短暂轻微体温升高(未超过40.5℃),所有猪只食欲和精神状态均快速恢复。
接种后病毒在血液中存在时间短,24天后即被清除,口腔和肛门拭子中病毒载量极低,表明病毒排出量少,传播风险小。同时,所有接种猪均产生了高水平的ASFV p30抗体。
最令人鼓舞的是,在接种27天后,用100 HAD₅₀剂量的原始强毒株进行攻毒,所有接种疫苗的猪均存活,且未出现发热或任何临床症状。而未接种的对照猪全部在11天内死亡。
病理学检查也显示,接种疫苗的猪器官无明显病变,病毒载量极低或检测不到,进一步证明了该疫苗候选株的安全性及保护效果。
激活先天与适应性免疫,无细胞因子风暴
通过转录组测序(RNA-seq)分析发现,该双缺失病毒能激活多条免疫通路,包括Toll样受体信号、RIG-I样受体信号、抗原呈递、B细胞受体信号等,说明其能同时激起先天免疫和适应性免疫。
值得注意的是,接种后并未引起IL-6、IL-12、IFN-α等关键炎症因子的剧烈释放,表明疫苗不会引发“细胞因子风暴”,接种后仅引发轻微炎症反应,动物整体耐受良好。
为非洲猪瘟防控提供新的疫苗候选株
该双基因缺失株HuBΔCD2vΔA137R不仅安全、免疫原性好,而且保护效果全面,攻毒后猪只无临床症状、无病毒大量复制,具备成为优质活疫苗的潜力。
目前,越南已批准一款缺失I177L基因的ASF减毒活疫苗上市,而我国自主研发的双基因缺失疫苗候选株的出现,标志着我们在ASF疫苗研发领域又迈出坚实一步。
研究人员表示,未来还将继续优化疫苗株,进一步删除其他毒力基因,以期获得更安全、更稳定的疫苗产品,为养猪业提供更可靠的防控利器。
非洲猪瘟的疫苗研发之路依然漫长,但每一项实质性进展都值得我们关注和期待。这款双基因缺失疫苗候选株的成功,不仅展示了我国科研团队的实力,也为全球ASF防控提供了新的思路与希望。
未来,随着进一步的中试和临床验证,有望推动该疫苗早日投入应用,帮助广大养殖户科学防控非洲猪瘟,守护猪群健康,稳定生猪生产,助力行业可持续发展。
农兜小程序
⇩⇩⇩
如在小程序使用中有任何建议和反馈,欢迎后台留言。
期待与您面对面地交流!
往期回顾








{{item.content}}